1月24日,中國國家藥監(jiān)局藥品審評中心(CDE)官網(wǎng)公示顯示���,默沙東(MSD)在中國遞交了1類新藥MK-6024注射液的臨床試驗申請,并獲得受理���。公開資料顯示��,MK-6024(efinopegdutide)是一款每周一次的GLP-1R/GCGR雙重激動劑����,目前在全球處于2期臨床試驗階段����。2020年8月,默沙東以高達8.7億美元獲得該產(chǎn)品在美國和全球開發(fā)和推廣的獨家許可���。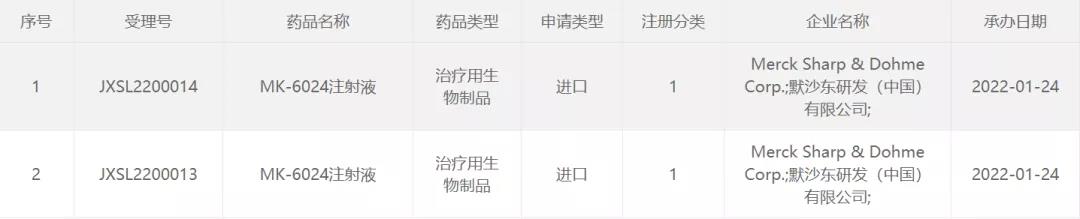
圖片來源:CDE官網(wǎng)截圖
GLP-1R和GCGR是G蛋白偶聯(lián)受體家族成員����,它們是維持人體血糖平衡的兩個重要“調(diào)節(jié)器”����。其中,GLP-1R是胰高血糖素樣肽-1(GLP-1)的受體����,主要在攝食后發(fā)揮作用���,通過與其配體GLP-1結合,刺激胰島素分泌��,使餐后血糖降低并維持在正常水平�����;GCGR是胰高血糖素(glucagon)的受體�,在饑餓狀態(tài)下,GCGR通過與其配體胰高血糖素結合來提高人體血糖水平�。研究表明,GLP-1R/GCGR雙重激動劑具有多種作用方式�,不但可以通過激活GLP-1R,提高胰島素分泌并且降低食物攝入����,而且可以通過激活GCGR起到降低炎癥和脂肪生成等效果�����。目前�����,GLP-1R/GCGR的雙重激動劑療法已成為治療糖尿病、肥胖�、非酒精性脂肪性肝炎(NASH)等疾病的一個新方向。Efinopegdutide正是韓美公司(Hanmi Pharmaceutical)開發(fā)的一款合成的�����、經(jīng)修飾的胃泌酸調(diào)節(jié)素(OXM)肽��。OXM是一種雙重激動劑���,作用于GLP-1R和GCGR�����。2020年8月��,默沙東以高達8.7億美元與韓美公司達成合作���,從而獲得該產(chǎn)品在美國和全球開發(fā)和推廣的獨家許可。公開資料顯示���,該產(chǎn)品此前已在多項1期和2期臨床試驗中評估了安全性和有效性�,包括治療伴有和不伴有2型糖尿病的重度肥胖患者。ClinicalTrials官網(wǎng)顯示��,默沙東正在開展一項efinopegdutide治療非酒精性脂肪肝的2期臨床試驗���。該臨床試驗將評估efinopegdutide與司美格魯肽相比治療NAFLD患者的療效��,評價標準是治療24周后��,患者肝臟脂肪含量的平均降低幅度����。公開資料顯示�����,隨著肥胖和代謝綜合征的流行�,非酒精性脂肪性肝(NAFLD,即常說的“脂肪肝”)已成為常見的慢性肝病之一���。其中NASH是NAFLD的一種進展形式,正在成為肝硬化和肝移植的主要原因之一����。希望默沙東的efinopegdutide在中國的臨床試驗申請早日獲批,并順利開展臨床研究,早日造?;颊摺?/span>



