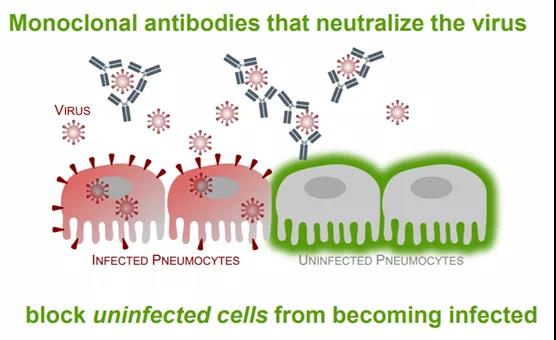
12月8日,騰盛博藥旗下控股公司騰盛華創(chuàng)抗新冠病毒中和抗體安巴韋單抗/羅米司韋單抗聯(lián)合療法(以前稱BRII-196/BRII-198聯(lián)合療法)獲中國國家藥品監(jiān)督管理局(NMPA)應急批準。該聯(lián)合療法的獲批不僅意味著中國迎來了首款新冠病毒中和抗體治療藥物,也標志著中國生物醫(yī)藥企業(yè)和科研人員在新冠中和抗體的研發(fā)中實現(xiàn)了“零”的突破。眾所周知���,一款新藥的誕生至少需要10年左右的時間����。而此次獲批的安巴韋單抗/羅米司韋單抗聯(lián)合療法從最初的實驗室研究到獲批僅用了不到20個月的時間����。那么��,這款新冠中和抗體聯(lián)合療法何以能在這么短的時間內獲批��?在疫情期間�����,它的開發(fā)又經歷了哪些特殊的挑戰(zhàn)�?本文中���,讓我們一起來回顧下中國首款新冠病毒中和抗體聯(lián)合治療藥物的誕生之旅���。時鐘撥回到2020年初的冬天�,一場突如其來的新冠疫情打亂了我們的正常生活。面對一種前所未知的新冠病毒���,許多生物醫(yī)藥公司和研究者都第一時間投身到了這場沒有硝煙的戰(zhàn)爭中�。小分子抗病毒藥物�����、新冠疫苗、中和抗體……���,科學家們紛紛從不同的領域著手�,以求盡快找到應對新冠疫情的方法�����,騰盛博藥就是其中的一員����。“騰盛博藥致力于針對重大感染性疾病以及其它重大公共衛(wèi)生疾病開發(fā)創(chuàng)新療法。在傳染病研究領域��,尤其是呼吸道病毒藥物研發(fā)領域����,我們擁有豐富的研究經驗。新冠疫情爆發(fā)后����,公司毫不猶豫地決定進行新冠中和抗體療法的開發(fā)�,希望用我們的所長為人類抗擊疫情貢獻一份力量?�!彬v盛博藥高級副總裁兼生物制藥部門負責人朱青博士在接受藥明康德內容團隊采訪表示。 提到中和抗體�����,大家最熟悉的可能是它的中和功能�。中和抗體通過與病毒表面的特異性抗原相結合,防止它們與細胞上表達的受體相結合并進入細胞����,進而防止病毒感染尚未受到感染的細胞。以針對新冠病毒的中和抗體為例�,多款抗體都靶向新冠病毒刺突蛋白的受體結合域(RBD)。RBD是刺突蛋白與細胞上的ACE2受體結合的關鍵蛋白域����,通過阻斷它們之間的相互作用可以防止新冠病毒感染人體細胞。▲中和抗體阻止病毒感染細胞示意圖(圖片來源:參考資料[4])談及中和抗體的優(yōu)勢�����,朱青博士表示:“與疫苗相比���,中和抗體不但可用于治療受到新冠病毒感染的患者��,而且能夠作為預防性療法��,給容易受到感染的高危人群提供被動免疫能力��。在預防性療法方面���,中和抗體的優(yōu)勢還體現(xiàn)在患者接受注射后能夠立即生效���,對那些不能對疫苗產生足夠免疫應答的人群(例如老年人和免疫系統(tǒng)受到抑制的患者)同樣有效?!?/span>為何從一開始就選擇了“雞尾酒”聯(lián)合療法,則是源于騰盛博藥團隊豐富的抗病毒藥物研發(fā)經驗��?���!靶鹿诓《臼荝NA病毒,從歷史經驗及病毒學原理來看��,RNA病毒的突變率一般都很高��,因此在設計之初����,我們就決定開發(fā)‘雞尾酒’療法����,也就是希望通過具有不同作用機制的中和抗體聯(lián)合用藥����,來預防未來可能會出現(xiàn)的病毒突變情況�����?��!敝烨嗖┦拷榻B道��。這是一個與時間賽跑的過程�����。為了能夠以最快的速度找到合適的中和抗體��,騰盛博藥決定通過合作來加快研發(fā)進程����。在快速調研后����,騰盛博藥發(fā)現(xiàn)清華大學張林琦教授與深圳市第三人民醫(yī)院張政教授的研究團隊已經從中國被治愈的COVID-19患者中發(fā)現(xiàn)了多個具有治療COVID-19潛力的全人源單克隆中和抗體����。于是���,三方很快建立了合作����,于2020年初共同成立騰盛華創(chuàng)以推動中和抗體的研發(fā)�。遠在美國的朱青博士也立刻趕回中國,日夜奮戰(zhàn)參與到研究中�。在多方的齊心協(xié)力下,研究人員終于篩選出了兩款具有不同結合位點的新冠中和抗體——安巴韋單抗和羅米司韋單抗��。據朱青博士介紹��,安巴韋單抗和羅米司韋單抗是兩款非競爭性結合新冠病毒刺突蛋白中和抗體��,對新冠病毒均具有高度中和活性��。此外�����,研究人員還應用了生物工程技術,以降低抗體介導依賴性增強作用的風險�����,并通過對每種抗體的可結晶片段區(qū)域(Fc段)進行修飾����,以延長抗體的半衰期��,以期獲得更持久的治療效果��。基于這樣的抗體設計�,由安巴韋單抗和羅米司韋單抗組成的“雞尾酒”療法可以非競爭性地識別新冠病毒刺突蛋白RBD中獨特的表位,減少在抗體治療過程中產生抗藥性病毒的機會����,進而增加抗體與未來病毒變種結合的可能性。2020年7月��,安巴韋單抗/羅米司韋單抗聯(lián)合療法的臨床試驗申請獲得中國國家藥監(jiān)局藥品審評中心(CDE)批準�����,成為了當時全球范圍內最早進入臨床試驗的新冠中和抗體之一�?���!?strong style="margin: 0px; padding: 0px; outline: 0px; max-width: 100%; box-sizing: border-box !important; overflow-wrap: break-word !important;">從抗體的最初篩選到開始人體試驗�����,我們只用了不到4個月時間����。在新藥研發(fā)領域,尤其是在抗病毒抗體的藥物研發(fā)領域�,這一速度幾乎是前所未有的?���!敝烨嗖┦可钣懈杏|地說到。通常情況下���,獲得臨床批件后,研究人員就可以招募患者開展臨床研究��。但隨著2020年7月中國的疫情得到基本控制,新冠患者越來越少�����,這意味著臨床試驗很難再招募到患者��。因此�����,騰盛博藥團隊決定暫停中國的臨床研究�,轉移至美國進行安巴韋單抗/羅米司韋單抗聯(lián)合療法的臨床試驗申請�。做出這個決定并不容易,因為這意味著人力�、物力、財力等多方面的壓力和挑戰(zhàn)���,但騰盛博藥團隊并沒有猶豫�����。2020年9月����,朱青博士回到美國,開始主導安巴韋單抗/羅米司韋單抗聯(lián)合療法的臨床申報和研究開展�。盡管彼時在美國開展新冠抗體臨床研究項目較多,患者招募面臨競爭壓力��,但得益于該聯(lián)合療法在健康人群中取得的良好安全性數據����,安巴韋單抗/羅米司韋單抗聯(lián)合療法得到了美國國立衛(wèi)生研究院(NIH)下屬的國家過敏和傳染病研究所(NIAID)的支持和資助,使得這一研究(ACTIV-2)得以快速推進�。ACTIV-2是一項全球多中心的2/3期臨床試驗,在美國�����、巴西�、南非、墨西哥���、阿根廷和菲律賓等全球多個臨床試驗中心開展��,其中3期臨床試驗部分在全球入組了847位受試者����。而今年6月以來,隨著中國新冠疫情在多地點狀出現(xiàn)���,騰盛博藥也在中國啟動了安巴韋單抗/羅米司韋單抗聯(lián)合療法在中國的2期臨床����。安巴韋單抗/羅米司韋單抗聯(lián)合療法的治療優(yōu)勢也在臨床試驗中得到了進一步的驗證�。ACTIV-2研究3期最終臨床試驗結果顯示:與安慰劑相比,安巴韋單抗/羅米司韋單抗聯(lián)合療法將臨床進展為重度疾病高風險的COVID-19門診患者的住院和死亡風險降低80%�;對早期開始接受治療(癥狀出現(xiàn)后5天內)的受試者,與晚期開始接受治療(癥狀出現(xiàn)后6至10天內)的受試者相比��,安巴韋單抗/羅米司韋單抗治療組均觀察到顯著的住院和死亡率降低����。而且�����,安巴韋單抗/羅米司韋單抗聯(lián)合療法在安全性上也顯著優(yōu)于安慰劑組���。在2021年9月30日舉辦的2021年美國感染性疾病周(IDWeek)年會上��,騰盛博藥通過口頭報告形式公布了ACTIV-2研究3期的出色中期數據��?���;谶@一積極的臨床試驗數據,騰盛博藥在今年10月初向美國FDA提交了安巴韋單抗/羅米司韋單抗聯(lián)合療法的緊急使用授權(EUA)申請���,并同步將3期臨床中期報告遞交中國國家藥監(jiān)局藥品審評中心(CDE)����。此次該聯(lián)合療法在中國被應急批準�����,用于治療輕型和普通型且伴有進展為重型(包括住院或死亡)高風險因素的成人和青少年(12-17歲��,體重≥40 kg)新型冠狀病毒感染(COVID-19)患者��。其中青少年(12-17歲����,體重≥40 kg)適應癥人群為附條件批準輕型和普通型且伴有進展為重型(包括住院或死亡)高風險因素的成人COVID-19患者,并附條件批準用于兒童(≥12歲�,體重≥40 kg)COVID-19患者。這一聯(lián)合療法在中國的獲批�,標志著中國擁有了首個自主研發(fā)并經過國際多中心大樣本隨機、雙盲、安慰劑對照研究證明有效的新冠病毒中和抗體聯(lián)合治療藥物�。而此時,距這款聯(lián)合療法最初的實驗室研究僅不到20個月的時間��。在朱青博士看來���,“這樣的速度不僅是基于騰盛博藥自身在抗病毒藥物領域擁有豐富的研發(fā)經驗和高效的執(zhí)行力���,更得益于科研院所、醫(yī)院��、CRO��、以及政府機構的之間的相互合作和支持”�����。眾所周知��,隨著疫情的延續(xù)����,新冠病毒也出現(xiàn)了許多變異株。如何應對新冠病毒變異株成為了行業(yè)面臨的又一挑戰(zhàn)。由于安巴韋單抗/羅米司韋單抗聯(lián)合療法的臨床研究比其它已獲FDA批準的新冠中和抗體晚了一些����,ACTIV-2試驗3期研究剛好入組了包括2021年1月至7月出現(xiàn)的新冠病毒變異株患者。作為3期研究分析的一部分����,研究人員也將評估安巴韋單抗/羅米司韋單抗聯(lián)合療法對不同類型新冠病毒變異株的臨床有效性。根據目前的體外嵌合病毒實驗數據�,安巴韋單抗/羅米司韋單抗聯(lián)合療法對廣受關注的主要病毒變異株均保持中和活性,包括“阿爾法”(Alpha)���、“貝塔”(Beta)����、“伽馬”(Gamma)�����、“伊普西龍”(Epsilon)��、“德爾塔”(Delta)�、“德爾塔+”(Delta Plus)、“拉姆達”(Lambda)�����、以及“繆”(Mu)。騰盛博藥也正在開展針對“奧米克戎(Omicron)變異株的測試���。尤其引人關注的是�,該聯(lián)合療法對今年流行的“德爾塔”變異株感染患者的治療效果�,已在一些臨床救治中得到初步驗證。今年6月以來�,中國多個城市曾出現(xiàn)“德爾塔”變異株感染患者。據騰盛博藥總裁兼大中華區(qū)總經理羅永慶先生介紹�����,騰盛博藥通過與中國政府部門和醫(yī)院合作���,捐贈了近3,000人份的安巴韋單抗和羅米司韋單抗����,涉及廣東省���、云南省����、江蘇省����、湖南省、河南省�、福建省、寧夏自治區(qū)�、甘肅省、內蒙古自治區(qū)����、黑龍江省、青海省�、貴州省及遼寧省,救治了近900例患者���。很多人好奇�����,在最初設計這款聯(lián)合療法的時候��,還沒有“德爾塔”變異株����,研究團隊是如何做到對“德爾塔”變異株的覆蓋的。但這對于騰盛博藥和朱青博士而言�����,并不意外�����?����!把芯吭O計之初�����,我們就考慮到了新冠病毒未來可能會出現(xiàn)變異�����,所以才篩選了兩個具有不同作用機制的中和抗體�����,開展聯(lián)合療法的研究?��,F(xiàn)在來看�����,我們當初的開發(fā)策略是非常正確的���。”朱青博士回應說�。騰盛博藥還將在中國開展進一步研究,旨在評估安巴韋單抗/羅米司韋單抗聯(lián)合療法在免疫抑制人群中的預防免疫增強作用��。新冠疫情的爆發(fā)���,尤其是新冠病毒的不斷變異���,給疫苗以及中和抗體的開發(fā)帶來了巨大的挑戰(zhàn)。而騰盛博藥和合作伙伴共同開發(fā)中和抗體聯(lián)合療法的曲折歷程�,正是這一時代背景下的縮影。回顧過往一年多的歷程�����,朱青博士經歷和見證了許多難忘且感動的故事:為了和時間賽跑�����,公司與合作伙伴、政府機構全力合作的畫面�;研究團隊不辭辛苦,夜以繼日工作的情形�;以及她在“隔離房”中寫申報材料的時光……,一切歷歷在目�。當下,人類與新冠病毒的斗爭還在持續(xù)�。在藥明康德2020年2月舉辦的“科學戰(zhàn)疫線上論壇”上,騰盛博藥聯(lián)合創(chuàng)始人兼首席執(zhí)行官(CEO)洪志博士曾表示����,“COVID-19的疫情提醒了所有人,傳染病不會從我們的生活中消失�,它們正在影響所有人的生活方式,我們必須學習如何做好準備和應對���。我認為����,沒有一個政府����,一個國家����,一個行業(yè)�,一個醫(yī)療保健系統(tǒng)可單獨完成這一任務,我們必須共同努力�����,更好地開展合作�����,共同應對這樣的公共衛(wèi)生危機��?���!?/span>回顧過去的兩年����,無論是新冠疫苗、中和抗體�,還是小分子抗病毒藥物,一次次創(chuàng)記錄的開發(fā)速度都離不開企業(yè)、科研院所���、CRO��、政府機構等之間的齊心協(xié)力合作�。騰盛博藥相信��,在社會各界人士的共同努力下�,人類一定能夠開發(fā)出應對新冠病毒不斷變異的疫苗和治療藥物,讓我們早日回歸正常的生活�!
文章來源:醫(yī)藥觀瀾